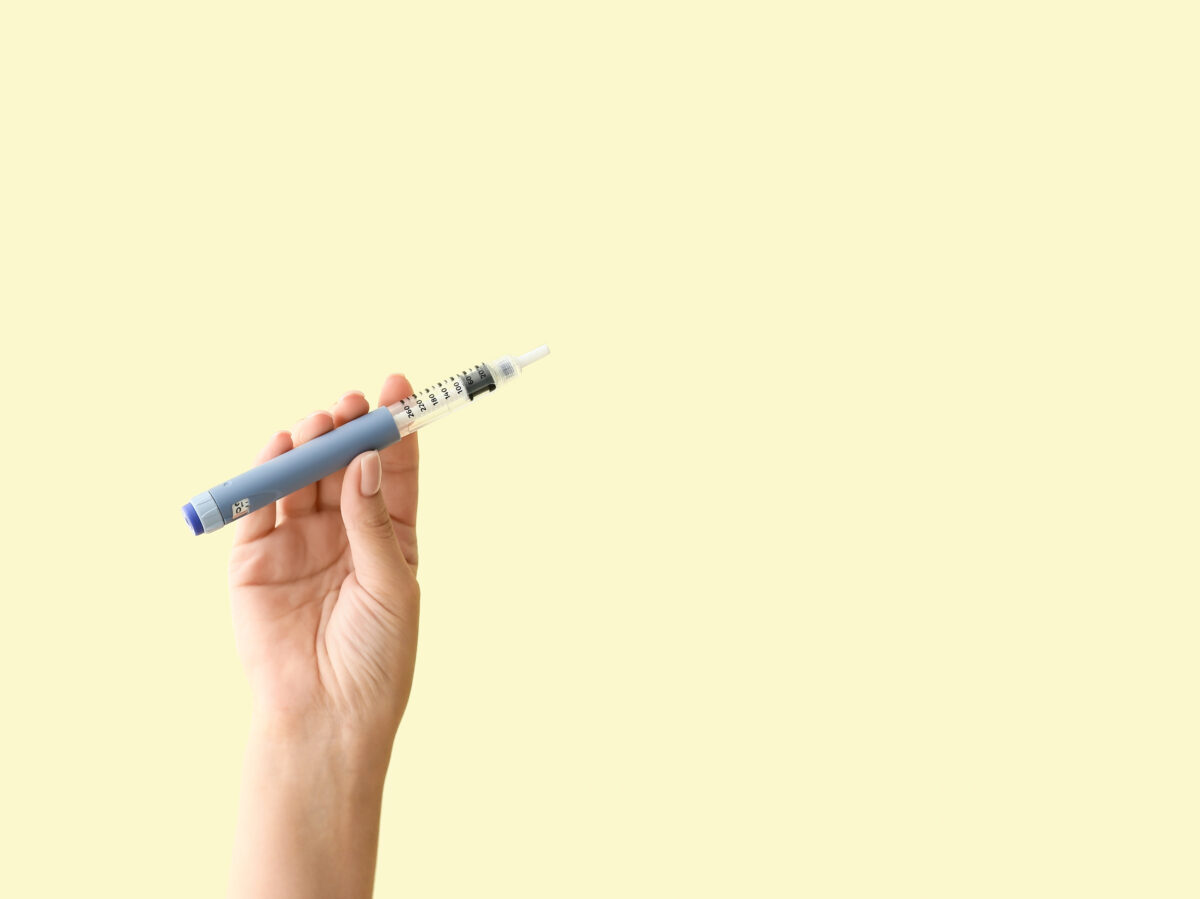
Semglee in englischer Aufmachung: Was gilt ab 31. Juli?
Bis zum 30. Juli darf Semglee 100 Einheiten/ml, Injektionslösung in einem Fertigpen (5x3ml), noch in englischer Aufmachung und Packungsbeilage in Verkehr gebracht werden. Was gilt, wenn Apotheken nach dem Stichtag noch Ware im Kühlschrank haben?
Weil Insulin glargin aufgrund von „Problemen beim sonstigen Hersteller“ von Lieferengpässen betroffen ist, konnte Biosimilar Collaborations Ireland Limited eine Ausnahmegenehmigung für Semglee erlangen. Das Bundesinstitut für Arzneimittel und Medizinprodukte (BfArM) hat eine drohende versorgungsrelevante Lieferengpasssituation festgestellt. „Nach aktuellen Lieferengpassmeldungen stehen wirkstoff- und darreichungsgleiche Arzneimittel bezogen auf die oben genannte Indikation derzeit nicht in einem den Bedarf deckendem Umfang zur Verfügung“, so das BfArM.
Insulin glargin ist ein langwirksames Insulin-Analogon und kommt als Basalinsulin zum Einsatz. Der Wirkstoff bindet an die Alpha-Untereinheit von Insulin-Rezeptoren und führt zu einer erhöhten Glukosespeicherung in den Zellen. Der Blutzuckerspiegel wird dadurch gesenkt. Die Verabreichung erfolgt einmal täglich immer zur gleichen Zeit. Als Nebenwirkungen drohen Hypoglykämie, lokale Hautreaktionen an der Einstichstelle, seltener auch Ödeme, Sehstörungen oder Myalgie.
Um den drohenden Engpass auf dem deutschen Markt abzuwenden, darf Semglee, das zur Behandlung von Diabetes mellitus bei Erwachsenen, Jugendlichen und Kindern ab einem Alter von zwei Jahren angewendet wird, in der für den irischen Markt bestimmten Kennzeichnung und entsprechender Packungsbeilage hierzulande zeitlich befristet in Verkehr gebracht werden. Gestattet ist dies bis zum 30. Juli. Dann soll die Verfügbarkeit von regulärer Ware in deutscher Aufmachung wieder gewährleistet sein.
Apotheken, die Semglee nach dem Stichtag noch vorrätig haben, müssen dennoch keine Kühlretoure anmelden. Der Grund: „Die beschiedene Befristung gilt für den Zulassungsinhaber, der auch Adressat des Bescheides ist“, teilt das BfArM mit. Bis zu diesem Zeitpunkt ist demnach dem Antragsteller erlaubt, die Ware in irischer Aufmachung abzugeben, beziehungsweise in Verkehr zu bringen. „Ware, die sich zu diesem Zeitpunkt bereits in der Distribution befindet, bleibt von der Befristung unberührt und gilt als rechtskräftig in Verkehr gebracht“, stellt das BfArM klar.
Außerdem besteht die Möglichkeit, dass die Ausnahmegenehmigung verlängert werden kann, sofern ein entsprechender Antrag eingereicht wurde. „Dabei ist zu beachten, dass eine Antragstellung lediglich dann vertretbar ist, wenn konkret Importware zur Verfügung steht und das Exportland durch die Verbringung in einen anderen Mitgliedstaat der EU keine Einschränkungen in der nationalen regulären Versorgung verzeichnen wird“, so das BfArM.
Mehr aus dieser Kategorie
Grippeimpfstoff 2025/26: Sanofi verlängert Bestellfrist
Seit Wochen wird zur Bestellung der Grippeimpfstoffe für die Saison 2025/26 aufgerufen, doch jetzt ist die Frist abgelaufen. Weil aber …
Bei Heuschnupfen Nasendusche?
Schon wieder läuft die Nase, wie ätzend! Das ist Alltag für alle, die von Heuschnupfen geplagt sind. Linderung ist da …
Jahresarbeitszeitkonto: Festgelegte Arbeitszeit entscheidend
Zum 1. August 2024 sind Änderungen in § 4 Bundesrahmentarifvertrag „Jahresarbeitszeitkonto“ in Kraft getreten. Demnach müssen Chef:innen die Arbeitsstunden nicht …