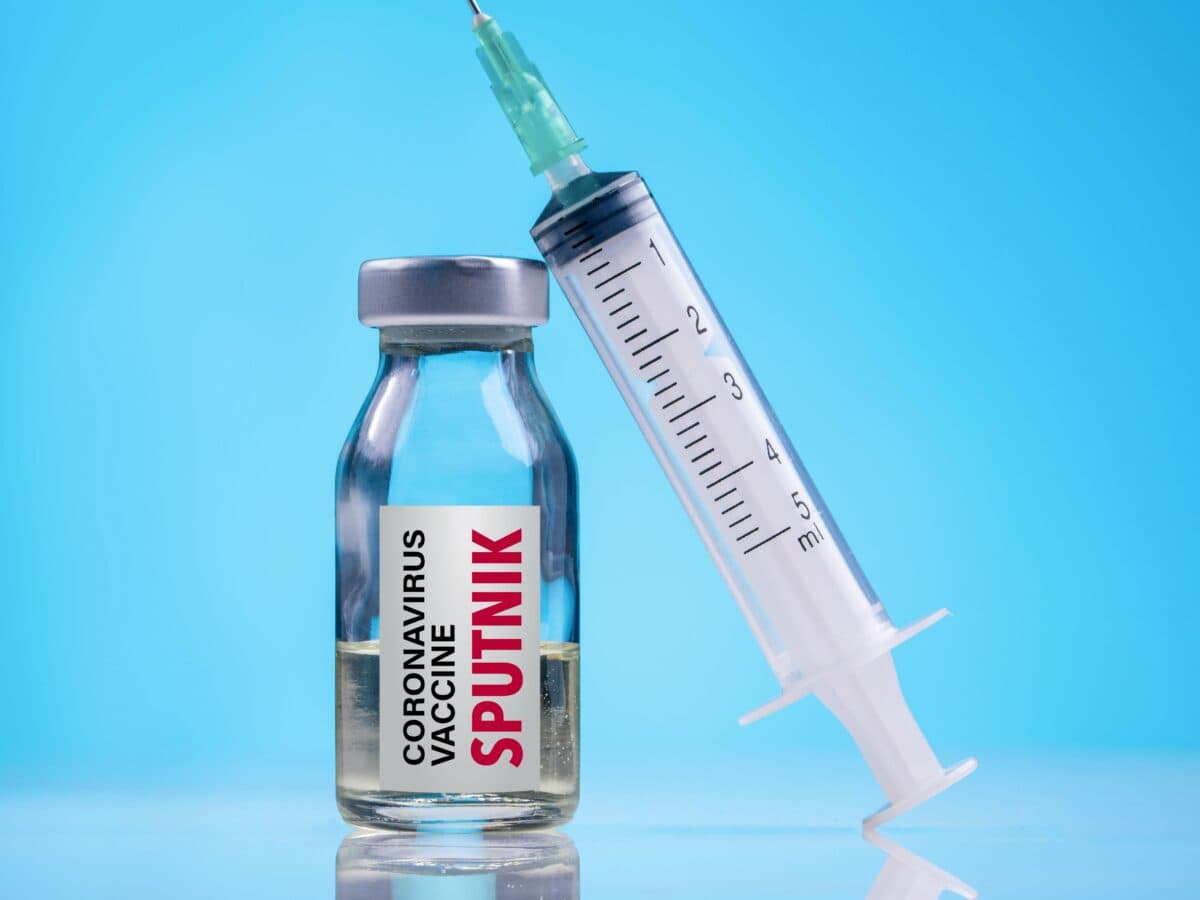
Kein Impfnachweis für Sputnik V, CoronaVac und Co.
Zwar hat die Ständige Impfkommission (STIKO) im Epidemiologischen Bulletin vom 31. März eine Empfehlung zur Corona-Impfung mit mRNA-Impfstoffen von Personen, die mit einem der nicht in der EU zugelassenen Ganzvirusimpfstoffe oder dem Vektor-basierten Impfstoff Sputnik V vorgeimpft wurden, veröffentlicht. Auf die Erstellung von Impfnachweisen hat die Empfehlung der Expert:innen aber keine Auswirkungen, wie der Apotheker-Verband Berlin klarstellt.
Bislang lautete die Empfehlung der STIKO: Alle Personen, die im Ausland mit einem nicht in der EU zugelassenen Impfstoff gegen Corona geimpft wurden, sollen eine neue Impfserie mit einem in der EU zugelassenen Impfstoff erhalten. Doch Ende März änderten die Expert:innen die Empfehlung, denn Daten zeigen, dass nach einer Grundimmunisierung mit einem inaktivierten Ganzvirusimpfstoff wie beispielsweise CoronaVac (Sinovac), Covilo (Sinopharm) und Covaxin (Bharat Biotech International Limited) eine Auffrischimpfung mit einem mRNA-Impfstoff genügt und der so erlangte Impfschutz mit dem nach einer Dreifachimpfung mit einer mRNA-Vakzine vergleichbar ist. Für den adenoviralen Vektor-Impfstoff Sputnik V (Gamaleja) liegen solche Daten bislang noch nicht vor.
Merke: Personen, die mit einem der genannten in der EU nicht zugelassenen Impfstoffe die Grundimmunisierung abgeschlossen haben, sollten laut STIKO mit einem Mindestabstand von drei Monaten zur letzten Impfung eine Auffrischimpfung mit einem mRNA-Impfstoff erhalten – Comirnaty (BioNTech) und Spikevax (Moderna) werden als gleichwertig angesehen.
Personen, die nur eine Impfdosis eines in der EU nicht zugelassenen Impfstoffes erhalten haben und somit die Grundimmunisierung nicht abgeschlossen haben, sollten laut Empfehlung der Expert:innen eine neue Impfserie bestehend aus Grundimmunisierung und Booster – gemäß der STIKO-Empfehlung – beginnen. Gleiches gilt für diejenigen, die mit einem anderen in der EU nicht zugelassenen Impfstoff immunisiert wurden.
„Die STIKO-Empfehlung hat keine unmittelbaren Auswirkungen auf die Erstellung von Covid-19-Zertifikaten“, stellt der Apotheker-Verband Berlin klar und verweist auf § 22a Infektionsschutzgesetz.
Gemäß § 22a IfSG ist ein Impfnachweis „ein Nachweis hinsichtlich des Vorliegens eines vollständigen Impfschutzes gegen das Coronavirus SARS-CoV-2“. Ein vollständiger Impfschutz liegt vor, wenn:
- die Einzelimpfungen mit einem oder verschiedenen Impfstoffen erfolgt sind, die
- von der EU zugelassen sind oder im Ausland zugelassen sind – letztere müssen von ihrer Formulierung her identisch mit einem in der EU zugelassenen Impfstoff sein,
- insgesamt drei Einzelimpfungen erfolgt sind und
- die letzte Einzelimpfung mindestens drei Monate nach der zweiten Einzelimpfung erfolgt ist.
„Die Zulassung des verwendeten Impfstoffes in der EU (bzw. dessen Identität hinsichtlich der Formulierung mit einem in der EU zugelassenen Impfstoff) ist danach zwingende Voraussetzung für einen gültigen Impfnachweis“, so der BAV. Sputnik V, CoronaVac, Covilo und Covaxin sind weder in der EU zugelassen noch mit einer der in der EU zugelassenen Vakzinen in ihrer Formulierung identisch.
Das könnte dich auch interessieren
Mehr aus dieser Kategorie
Lieferengpass und Dringlichkeitsliste: Neue Regeln beim E-Rezept
Beim E-Rezept gelten seit dem 15. April neue Dokumentationsregeln für Abweichungen von der Verordnung aufgrund eines Lieferengpasses und für Arzneimittel …
Pflegehilfsmittel: Neuer Vertrag gilt ab Juni
Apotheken, die auch nach dem 31. Mai Versicherte mit Pflegehilfsmitteln zum Verbrauch versorgen wollen, müssen dem neuen Vertrag beitreten. Eine …
Herstellerrabatt: AOK retaxiert Mounjaro
Die AOK Sachsen-Anhalt verschickt derzeit Mounjaro-Retaxationen über den Herstellerrabatt. Der Grund ist ein technischer Fehler in der Adba-Datenbank. Retaxiert werden Mounjaro-Verordnungen, …